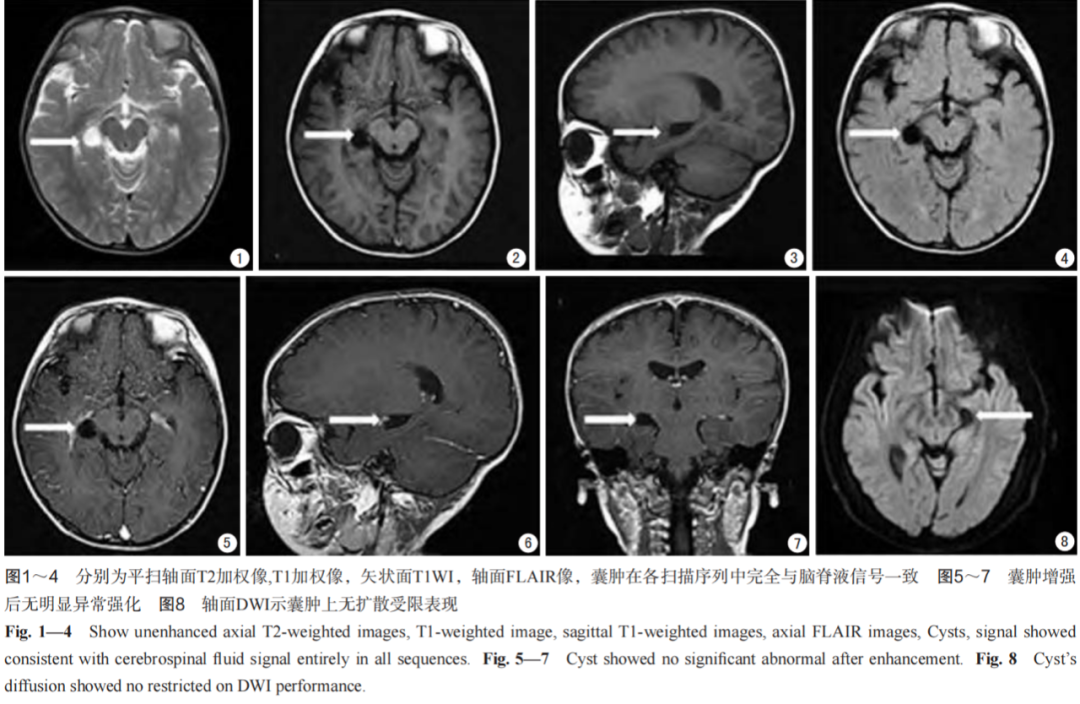
肝细胞癌(hepatocellular carcinoma,HCC)是我国常见的恶性肿瘤及第2位肿瘤的致死病因,治疗手段主要为肝切除和肝移植。肝移植存在诸多限制,如缺少供体肝源、等待时间较长、经济条件限制、术后需长期服用抗排异药物等。
肝静脉是肝脏血液的唯一出肝通道,如肝静脉受阻,其所引流的肝实质也会发生淤血。我国HCC病人大多数有肝硬化病史,需要在保证肿瘤完整根治性切除的前提下,保留更多的肝实质,减少术后肝功能衰竭的发生率。
传统观点认为,如果HCC侵犯主肝静脉时,主肝静脉所引流的全部肝段也应一并切除。对于HCC侵犯肝左静脉的患者,既往通常选择左半肝切除术以避免肝脏S3段静脉血液回流受阻。这是由于切除肝左静脉后,肝脏S3段静脉血液回流被完全阻断,导致肝脏S3段淤血。
脐裂静脉(umbilical fissure vein,UFV)是左半肝内的一个重要静脉分支,沿相邻脐裂1cm处走行,主要引流肝脏S3和S4段的静脉血液,大部分汇入肝左静脉(left hepatic vein ,LHV),少部分汇入肝中静脉(middle hepatic vein ,MHV)或MHV、LHV共干处。
1、 UFV的发生率
UFV的发生率约为72.8%-91.6%,并非存在于所有个体中,因检查方法、样本数量、样本中的个体差异、CT质量、造影剂时间而有所不同。
2、 UFV的分型

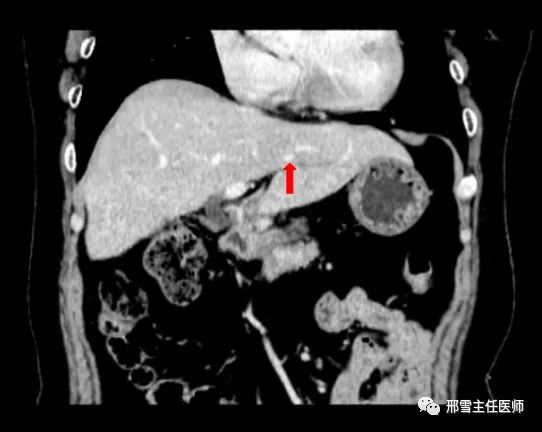
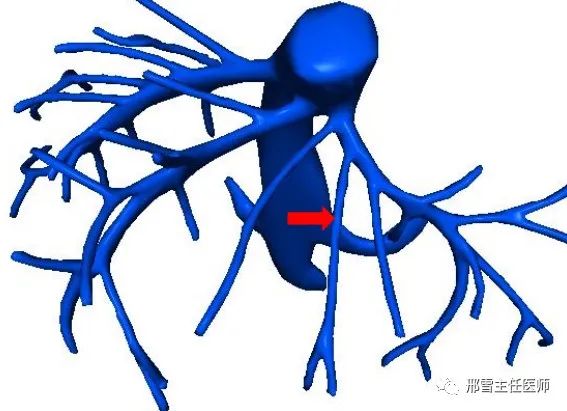
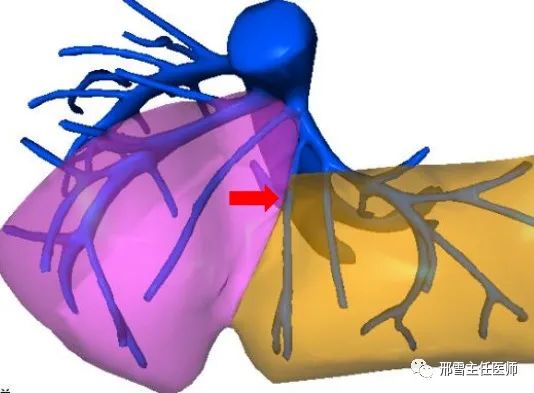
Ⅰ型:UFV汇入LHV(红色箭头所示为UFV,粉色区域为肝脏S4段,黄色区域为肝脏S3段,下同)
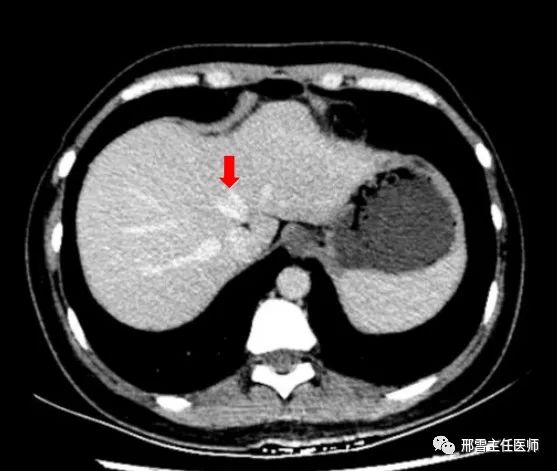

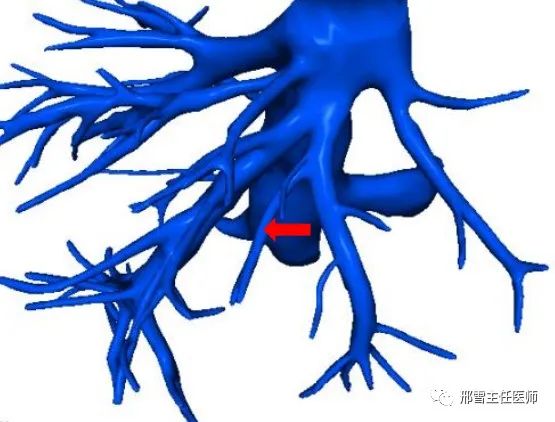
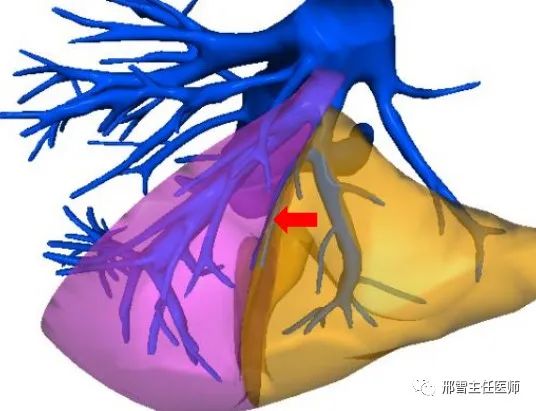
Ⅱ型:UFV汇入MHV
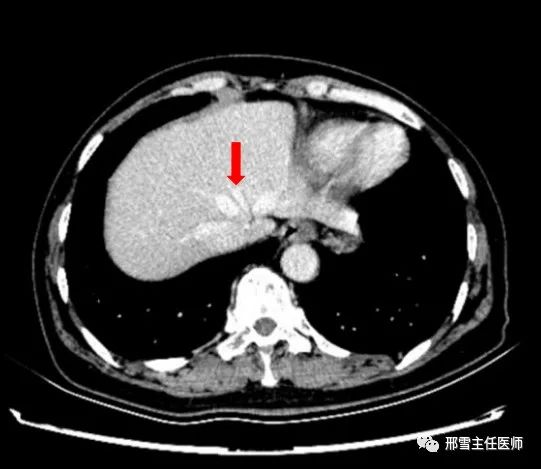
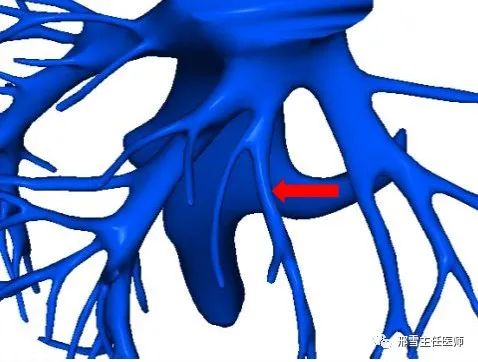
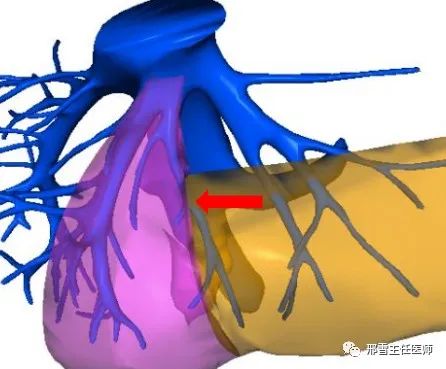
Ⅲ型:UFV汇入MHV与LHV共干处
3、识别UFV的临床意义
UFV是左肝内一条重要的肝静脉属支,主要引流S3、S4段肝静脉血液。UFV可以在肝切除术前做为解剖学标志,在肝脏实质离断过程中显露UFV有助于提示已临近主要肝静脉(LHV、MHV)和下腔静脉平面,此时应小心操作,以免损伤肝静脉和下腔静脉。
大多数情况下,UFV进入LHV或LHV与MHV汇合处。即使UFV汇入MHV,只要不靠近MHV根部结扎,就不会阻碍UFV回流。
当S2段肿瘤侵犯LHV时,如果选择施行左半肝切除术,势必牺牲无肿瘤侵犯的S3段正常的肝实质。
选择S2段合并LHV的切除,保留UFV在技术上是可行的,这种方式可以在保证肿瘤根治性切除的前提下保存完整功能的S3段,从而保留更多肝实质。
4、UFV在限量肝切除术中的应用
术前影像学检查确定UFV的存在,对位于S2段的HCC和结直肠癌肝转移并浸润LHV主干的病人,若计划施行扩大S2段切除和限量S4段切除,可以在切除LHV的同时保留S3段肝实质,残留的S3段静脉血液由UFV引流。
Kobayashi报告3例扩大S2段联合LHV切除而保留S3段。
Pringle法阻断入肝血流,从S2 和S3段边界的左缘离断肝实质,沿脐部向上分离,在S2段Glisson蒂根部结扎并切断,继续向LHV和UFV交汇处离断肝实质并显露UFV,完整切除S2段保留S3段。
S3段表面无瘀血表现,超声显示门静脉血流正常。术后复查S3段肝脏再生明显。
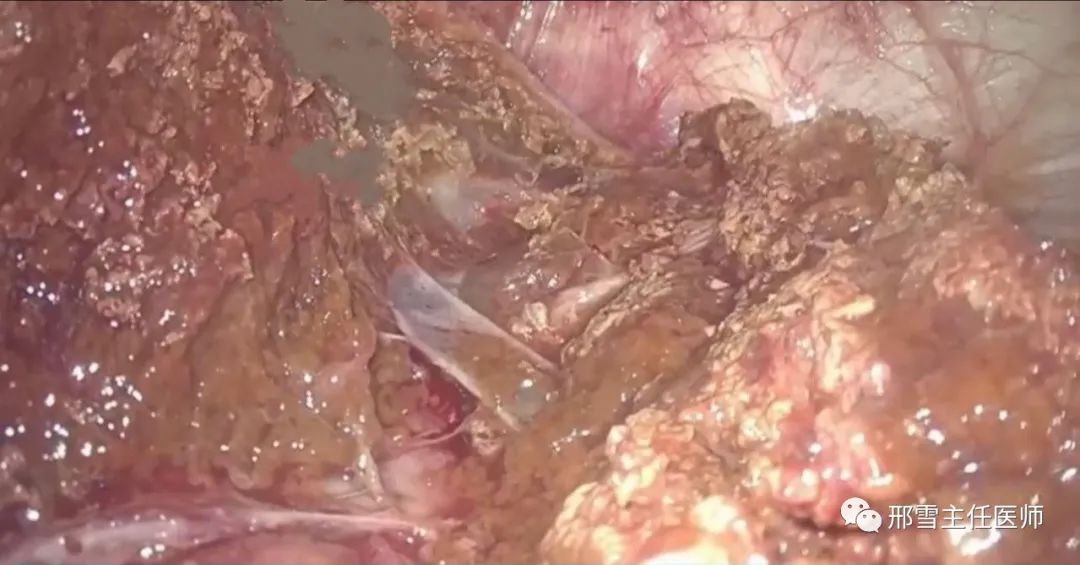
UFV术中所见
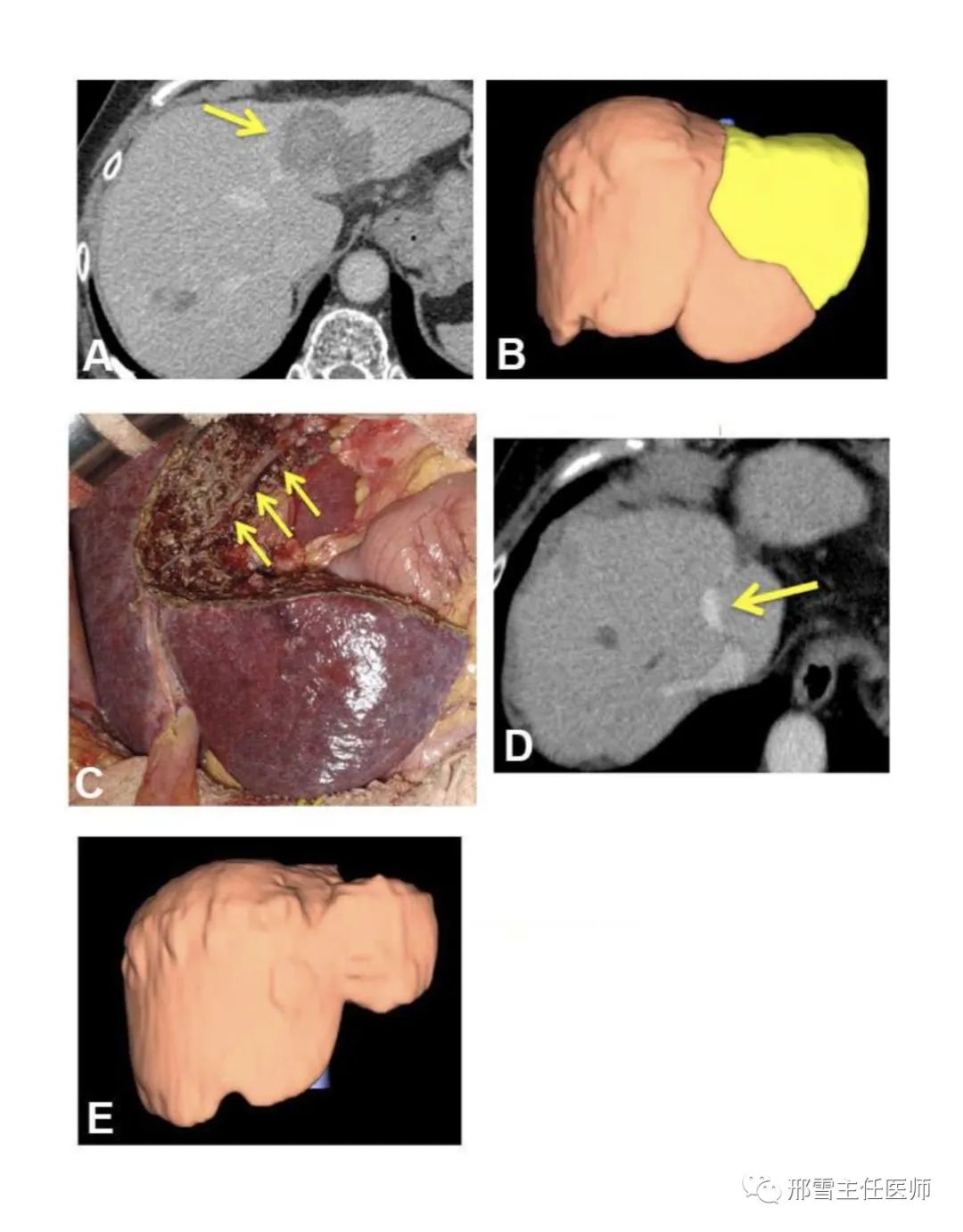
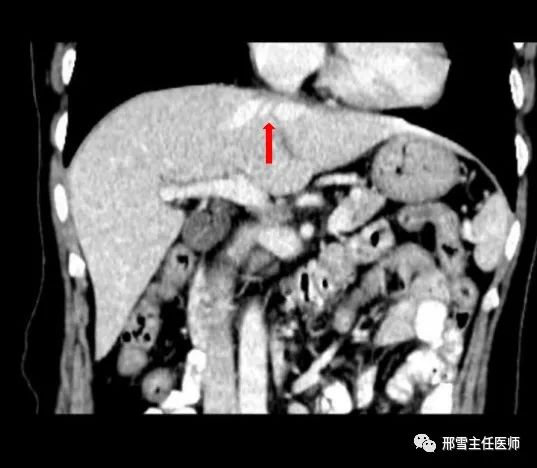
例1,(A)增强CT显示位于II段的HCC (箭头)并浸润LHV。(B)三维重建后预计肝切除界限和肝脏体积。(C)肝切除术后所见。肝断面显露UFV(箭头)。(D)术后增强CT显示通畅的UFV(箭头),III段无异常的增强影像。(E)肝切除术后3个月肝脏三维重建图像。尽管术后肝脏总体积小于术前,但术后III段体积是术前的108.6%。(图片来源:Kobayashi K,et al.J Am Coll Surg. 2017;225(3):e5-e11)
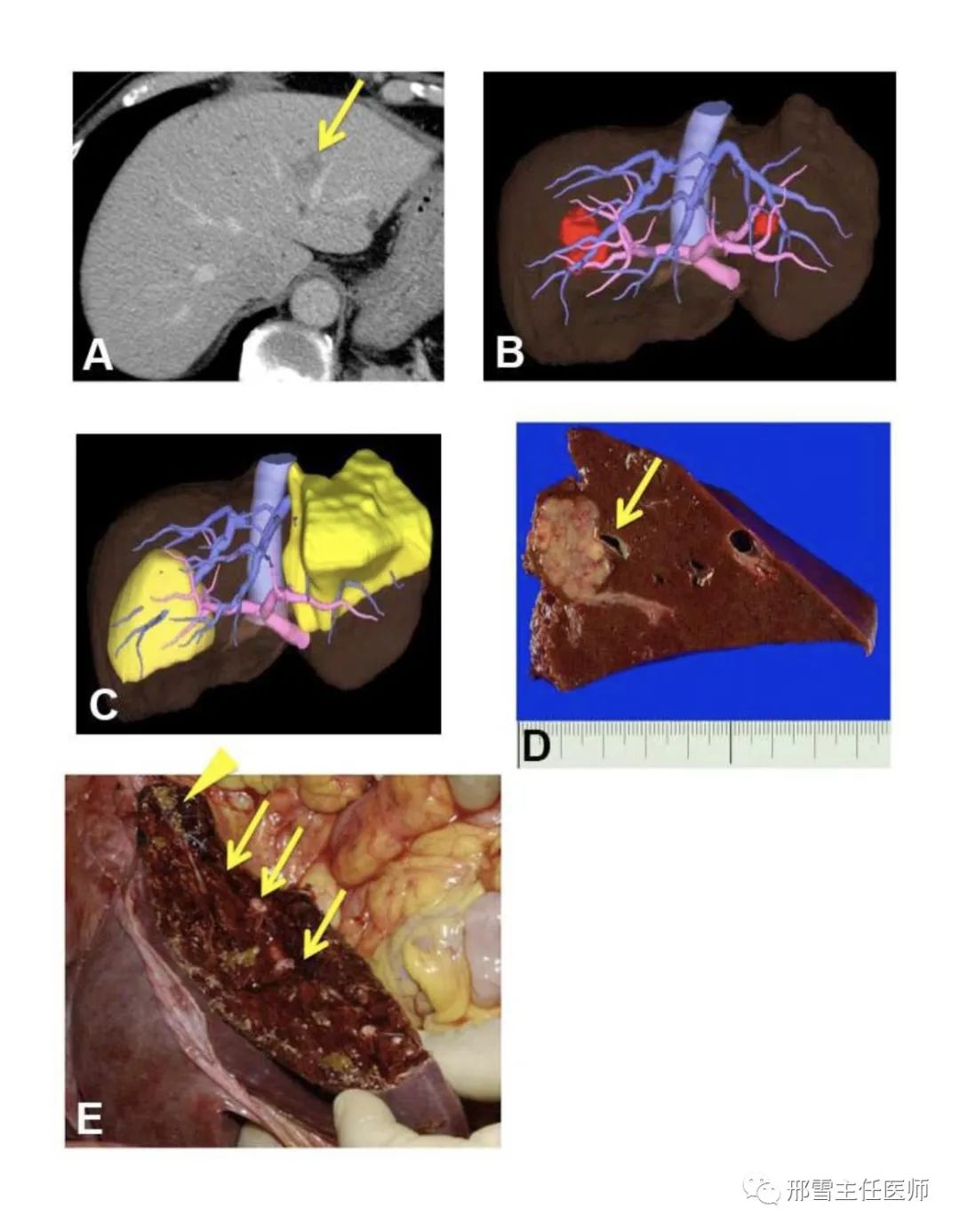
例2,(A)增强CT显示位于II段的结直肠癌肝转移(箭头)并侵犯LHV。(B)肝脏和肿瘤的术前三维重建图像。(C) 三维重建后预计肝切除界限和肝脏体积。计划施行扩大II段切除和限量IV段切除。(D)切除标本显示LHV被肿瘤浸润(箭头),手术切缘阴性。(E)肝切除术后所见,肝断面显露UFV(箭头)和LHV残端(箭头)。(图片来源:Kobayashi K,et al.J Am Coll Surg. 2017;225(3):e5-e11)
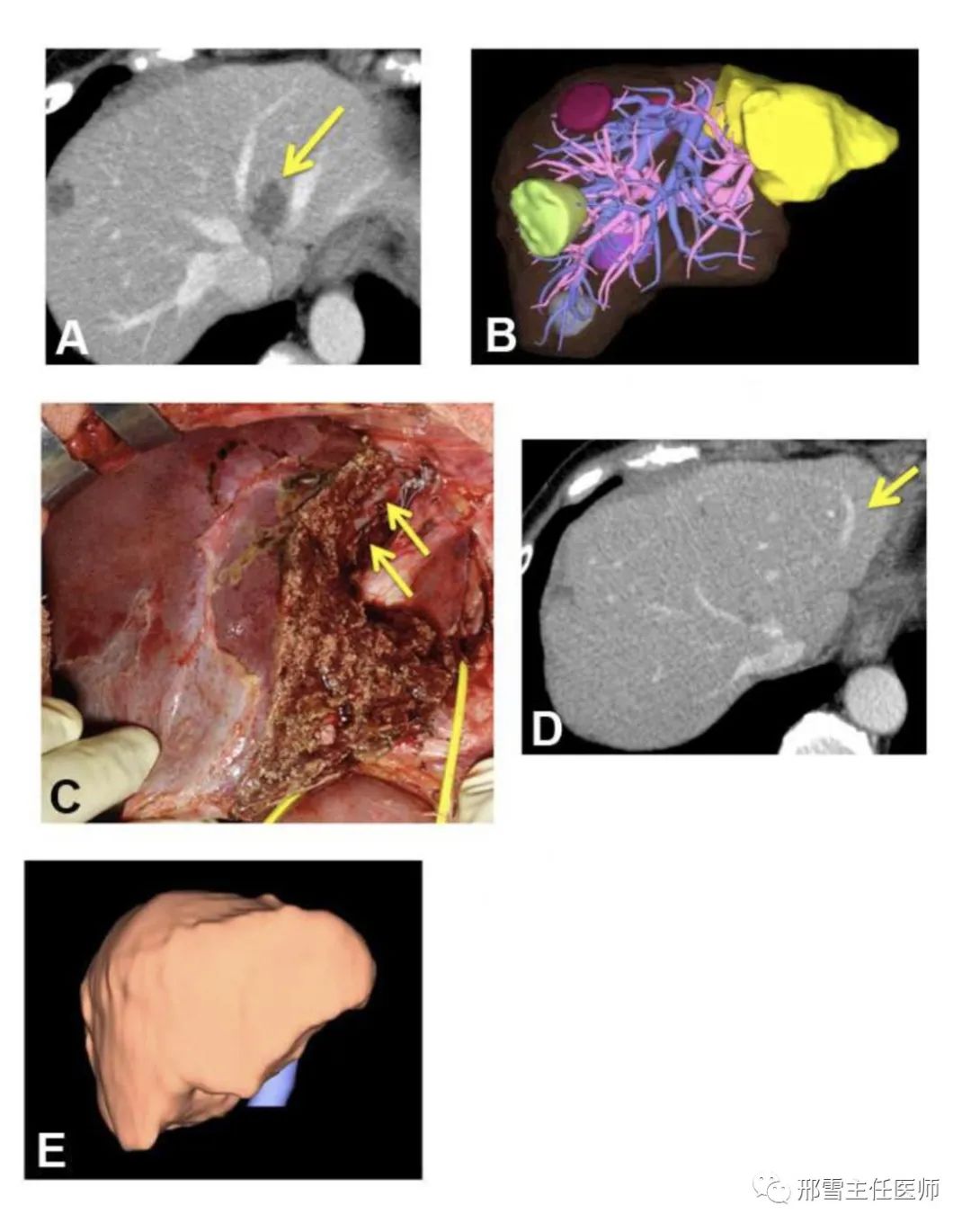
例3,(A)增强CT显示位于II段的结直肠癌肝转移(箭头)并侵犯LHV。(B)三维重建后预计肝切除界限和肝脏体积,计划施行8个肿瘤切除的扩大II 段切除和限量肝切除。(C) 肝切除术后所见,肝断面显露UFV(箭头)。(D)术后增强CT显示通畅的UFV(箭头),III段未观察到异常的增强模式。(E)肝切除术后3个月肝脏三维重建图像。尽管术后肝脏总体积小于术前,但术后III段体积是术前的137.2%。(图片来源:Kobayashi K, et al.J Am Coll Surg. 2017;225(3):e5-e11)
肝肿瘤复发施行反复肝切除具有很高的存活率,残留肝实质和主要血管的保留对术后肿瘤复发病人提高了重复肝切除的机会。
肿瘤仅限于S2段并浸润LHV,病人肝功能受损和/或肿瘤多发并且不能耐受左半肝切除,此术式被认为是最佳手术选择。
此术式明显提高复发性HCC反复干预的可能,不影响初始手术的根治效果。
因此,术前影像学检查辨别病人是否存在UFV具有重要的临床意义。
参考文献
[1]原发性肝癌诊疗规范(年版)编写专家委员会.原发性肝癌诊疗规范(2019年版)[J].中国临床医学,2020,027(001):140-156.
[2] Kwak BJ, Kim DG, Han JH, et al. Clinical outcome of 1,000 consecutive cases of liver transplantation: a single center experience. Ann Surg Treat Res. 2018 Nov;95(5):267-277.
[3]肖朝辉,文天夫.肝切除术后死亡因素及其防治[J].中国普外基础与临床杂志,2008(02):143-146.
[4] Hwang S, Lee SG, Park KM, et al. Quilt venoplasty using recipient saphenous vein graft for reconstruction of multiple short hepatic veins in right liver grafts. Liver Transpl, 2005, 11(1): 104-107.
[5]谢于,王振海,张东坡,等.可视化3D影像辅助下对肝脐裂静脉的认识[J].中国临床解剖学杂志,2020,38(05):559-561.
[6] Zhang J, Guo X, Qiao Q, et al. anatomical study of the hepatic veins in segment 4 of the liver using three-dimensional visualization. Front Surg. 2021 Aug 3;8:702280.
[7] Idrees M, Zhang L, Al-Ogaili Z, et al. Umbilical fissure vein, anatomical variation and potential surgical application. ANZ J Surg.2021 Jul;91(7-8):E479-E483.
[8] Kobayashi K, Hasegawa K, Kokudo T, et al. Extended segmentectomy II to left hepatic vein: importance of preserving umbilical fissure vein to avoid congestion of segment III. J Am Coll Surg. 2017 Sep;225(3):e5-e11.
限 时 特 惠: 本站每日持续更新海量各大内部创业教程,一年会员只需98元,全站资源免费下载 点击查看详情
站 长 微 信: lzxmw777