
在特异性RET抑制剂上市前,除了,多激酶抑制剂作为“靶向药物”也是这类患者的重要选择,本文我们将就多靶点激酶抑制剂(MKIs,multi-kinase inhibitors)的研究现状与进展进行盘点。
Session1
认识MKIs
随着基因组学、分子、细胞生物学和生物信息学快速发展,临床对肿瘤的认识越来越深入。基于肿瘤发生和发展的复杂性,绝大部分的肿瘤不是依靠一条信号通路维持生长和存活的,信号通路之间往往存在交叉和代偿。因此,在药物研发过程中,研究者提出了一个新的概念——多靶标酪氨酸激酶抑制策略, 即通过抑制多重信号通路或一条信号通路上下游多个分子达到协同治疗和克服耐药的双重功能。
伴随这一概念的提出,一些药物取得了一定的疗效并获得FDA的批准。索拉非尼是首个获批的MKI,用于不能手术肾细胞癌的治疗。从已获批的MKIs靶点分析看,其主要发挥作用的机制是通过抑制VEGFR信号通路抑制血管生成,同时通过抑制其他信号通路达到抗肿瘤的效果。目前已经有多个MKI药物获得FDA或NMPA批准应用于抗肿瘤治疗,治疗无需检测生物标志物。
表:常见的MKIs的靶点与适应证

Session 2
MKIs与RET基因
MKIs抗肿瘤的重要机制之一为通过抑制VEGFR信号通路抑制血管生成,从已获批的药物可以看到多数的MKIs的靶点都包含RET,这也许可以从分子结构做一些解释,同时也可以解释为什么已经开发的特异性抑制剂也很难避免会带来由于抑制VEGFR信号通路带来的高血压等不良反应。从RET蛋白晶体结构分析发现,在ATP结合位点,RET和VEGFR2 只有10%的氨基酸残基不同,而70%的氨基酸残基完全相同8,高度相似的ATP结合位点,为特异性药物研发带来挑战,同时在特异性药物开发出来前,多激酶抑制剂也给患者带来更多治疗的选择。
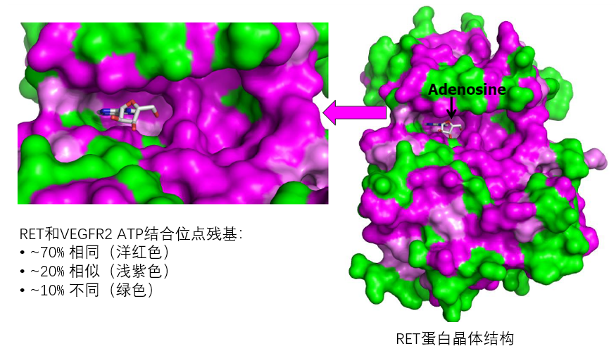
图:RET和VEGFR2结构具有高度相似性 8
因此在确定RET为肿瘤驱动基因后,多个MKIs在RET变异肿瘤如甲状腺癌和肺癌中进行了尝试。其中,Cabozantinib和Vandetanib在甲状腺癌临床试验取得了成功并获得FDA批准用于甲状腺癌治疗(与生物标志物无关);但这两种药物在RET融合肺癌患者中的尝试均以失败告终,没有获得肺癌相关的适应证。
Session 3
MKIs对于RET融合NSCLC
疗效和安全性如何?
虽然MKIs并未在RET融合NSCLC治疗上获得相应的适应证,但在临床实践中,没有更多药物选择的情况下,MKIs也给临床治疗增加了更多的选择性。那么MKIs对于 RET融合NSCLC患者的疗效和安全性如何?我们梳理了现有的研究数据,供大家参考。
多项II期单臂研究主要入组后线患者,ORR为16~53%,mPFS为4.5~7.3个月,总生存期小于1年1-4,10。在RET融合NSCLC,KIF5B融合伴侣占比超过70%,那么MKIs对不同融合伴侣疗效如何?Toyoaki Hida等的研究显示,仑伐替尼在CCDC6-RET融合患者中的疾病控制率(DCR,91.7% vs 61.5%)、临床受益率(CBR,66.7% vs. 30.8%)以及mPFS(9.1个月 vs. 3.6个月)均优于KIF5B-RET融合患者1。在Kiyotaka Yoh等的研究中,Vandetanib在不同RET融合类型中也显示出了疗效差异性,CCDC6-RET组的mPFS以及12个月总生存率分别为8.3个月及67%,而KIF5B-RET组分别为2.9个月及42%3。MKIs对主要KIF5B疗效明显差于非KIF5B患者。
此外,由于MKIs治疗导致了多种不良事件 (AE),这些 AE与其脱靶效应密切相关1-4,10。这些药物相关毒性限制了前瞻性临床试验中MKIs的长期给药剂量,减量率为 23~79%,停药率为 6~21。
表:MKIs用于RET融合阳性NSCLC的疗效
与AE数据汇总1-4,9,10
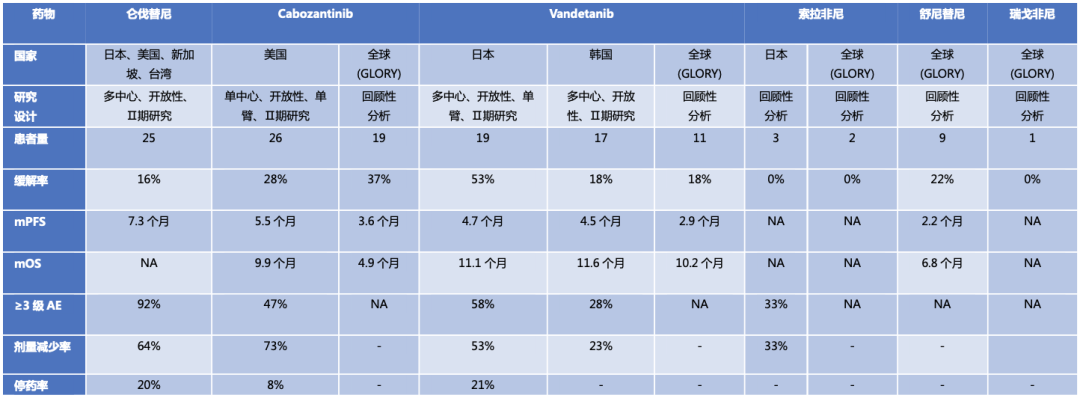
那么,MKIs对RET融合NSCLC患者一线治疗疗效如何?2017年,研究者对全球多中心RET注册库(GLORY)的数据进行了回顾性分析,该中心收集了165例RET重排NSCLC患者治疗的经验,其中53例未经TKI治疗的患者接受了MKIs治疗。结果显示,接受MKIs(Cabozantinib、Vandetanib以及舒尼替尼等)治疗患者的mPFS为 2.3个月,mOS为 6.8个月9。而在84例一线接受以铂类为基础的化疗的晚期初诊和RET重排的NSCLC患者中,其mPFS为7.8个月,mOS为24.8个月。基于以上结果,Oliver Gautschi等认为对于RET重排肺癌患者,含铂化疗的生存获益优于MKIs 9。
图:GLORY回顾性分析生存数据
(A) 任何抗RET的多激酶抑制剂的PFS; (B) Cabozantinib、vandetanib或舒尼替尼的PFS;(C) 任何抗RET的多激酶抑制剂的OS; (D) Cabozantinib、vandetanib或舒尼替尼的OS
在另一项中国开展的多中心、回顾性研究中,RET重排晚期NSCLC患者分别接受MKIs、免疫检查点抑制剂和化疗治疗。结果显示,接受MKIs的患者中位PFS为3.8个月,与全球数据基本一致12。此外,仍有两项卡博替尼用于RET融合NSCLC的研究也正在开展13,14。
整体来说,多激酶抑制剂在无论在一线还是后线,都没有带来更多获益。
Session 4
MKIs的局限性
MKIs虽然有一定的疗效,但由于无法主要精准抑制RET基因,其在RET融合阳性NSCLC中的应用会受到一定限制。
4.1
疗效限制
Alexander Drilon等对MKI类“靶向药物”和特异性TKI(EGFR/ALK /ROS1 TKI )的疗效通过气泡图进行了对比,如下图所示,MKIs用于RET融合阳性的NSCLC患者,ORR为20~30%,远低于EGFR/ALK/ROS1 TKI ORR>50%,中位PFS为2.7~7.3个月短于特异性TKI 9.7~25.8个月1-4,10,很显然MKI并未达到靶向药物应有的疗效。而现有的临床研究数据显示,特异性RET抑制剂普拉替尼对经铂类化疗人群患者的ORR为62%,中位PFS为16.5个月,初治患者ORR为88%,PFS未达到15,满足靶向药物疗效要求。
图:不同靶点靶向治疗的疗效比较
按照MKIs的研发思路,为什么多激酶通过多个信号通路的抑制反而疗效并没有达到预期?这里编者认为可能与肿瘤的异质性相关,在有明确驱动基因突变的肿瘤中,强力抑制驱动基因,可以达到比较好的疗效。若没有明确驱动基因突变的肿瘤中,多激酶的抑制思路,可能不失为一个好的选择。
4.2
安全性限制
如前所述,许多MKIs对除RET外的靶点,如VEGFR2等也有抑制作用。然而,与 VEGFR2 相比,这些药物靶向 RET 的能力更有限。因此,在临床可达到的血浆浓度下,Cabozantinib和Vandetanib 能更有效地抑制 VEGFR2而非RET。总体而言,目前可用的 MKIs 具有显著的脱靶效应11。
脱靶效应导致的药物相关不良事件包括:VEGFR2抑制引起的高血压、手足综合征和蛋白尿;EGFR 或 BRAF 抑制引起的皮疹;KIT 抑制引起的色素沉着;hERG 抑制引起的 QT间期延长;以及 EGFR 抑制的结果引起的腹泻等。这些药物相关毒性限制了MKIs的长期给药剂量,因此,无法保证其在部分患者中的使用或导致药物治疗剂量的不足,进一步影响治疗疗效11。
4.3
耐药性限制
此外, MKIs还存在固有耐药和获得性耐药,这也限制了它们在 RET融合阳性NSCLC中的临床应用。固有耐药可能是由上游伴侣基因 KIF5B 和 RET 融合引起的,RET上游KIF5B的存在导致RET转录显著增加,可能会增加克服嵌合RET癌蛋白需要的酪氨酸激酶抑制的量。而MKIs的获得性耐药可能来自特定的 RET 突变,如Cabozantinib和Vandetanib对门卫突变( V804M 和 V804L)的 NSCLC 患者无效17。
小结
自1980年代,RET被确认为一种癌基因并开始了大量研究。MKIs通过同时靶向多种细胞激酶来发挥抗肿瘤活性,尽管具有一定的RET激酶抑制活性,但疗效并未达到靶向治疗预期,且由于脱靶效应导致了多种AE的发生,此外MKIs还存在一定的耐药性,限制了其使用范围。
由于RET变异肿瘤存在大量未被满足的临床需求,推动特异性RET抑制剂研发。ARROW研究数据显示,特异性RET抑制剂普拉替尼在经治和初治RET融合阳性的NSCLC患者的ORR为62%和88%,经治患者的中位PFS为16.5个月。基于该研究的优异结果,2021年3月,普拉替尼在中国上市。从MKIs再发展至现在的特异性RET抑制剂,RET融合阳性NSCLC的治疗不断朝着更加精准的方向发展。
专家简介

刘喆 教授
首都医科大学附属北京胸科医院
专家点评
Q1
基于以上文章,结合您的临床实践,请您分享一下您对RET融合基因阳性NSCLC患者采用MKIs的治疗经验?
目前,大多数抗RET的药物都是MKIs。在特异性RET抑制剂获批以前,RET融合基因阳性NSCLC患者可能会接受化疗或免疫治疗。然而,这两种治疗的OS和PFS并不是非常理想。自2016年来,陆续有MKIs治疗RET融合基因阳性NSCLC的研究结果发布1-4,10。从现有的研究数据来看,这些药物均显示出了一定的临床活性。然而,与众所周知的 EGFR、ALK 和 ROS1 的 TKI 相比,其ORR和PFS仍然较低。MKIs可有效抑制非RET靶点,如VEGFR2、KIT、BRAF等,使患者“脱靶效应” 风险增加,同时由于MKIs非选择性而产生的药物相关毒性,都极大地限制了MKIs在RET融合基因阳性NSCLC中的疗效11。
在临床实践中,掌握MKIs治疗相关毒性的病因、治疗及全程管理尤为重要。只有更好地了解MKIs所至毒性的发生及发展机制才能制定出合理地预防及治疗策略,为合理地解决这个问题需要更多的临床研究提供数据支持。此外,晚期肿瘤通常会找到逃避靶点抑制的途径,从而导致耐药性,如何有效地处理MKIs的耐药问题也已成为一项重大挑战。
Q2
您如何看待RET融合阳性NSCLC患者治疗未来的发展方向?
最近,特异性RET抑制剂普拉替尼表现出显著的疗效,并已在中国获批上市,为患者带来了新的生存希望15。对于RET融合阳性NSCLC患者治疗未来的发展方向,一方面,研究者将进一步探索 MKIs 或特异性 RET 抑制剂对特定类型的 RET 融合的有效性,这有助于临床医生为不同患者选择最合适的治疗方法。另一方面,RET为罕见靶点,如何高效的筛选出潜在患者至关重要,首先建议所有的晚期患者在诊断时应该同时进行RET融合基因的检测,多基因共检,是未来的发展趋势,第二就是选择高效的检测方法,基于多基因检测要求,多重PCR检测和二代测序是目前晚期NSCLC患者分子诊断的合适选择,PCR法以周期短为优势,基于DNA和RNA层面的二代测序以同时可检测更多融合基因信息给临床治疗带来指导被临床认可。
最后,实现这些患者的长生存是终极目标,我们要用好手中的药物,做好“排兵布阵”,有靶打靶,让好药发挥更大的价值,让更少的患者“陪跑”,患者生存获益最大化。
附录:
表:MKIs用于RET融合阳性NSCLC正在进行的研究汇总

参考文献:
1.Hida T, Velcheti V,Reckamp KL, et al.A Phase 2 Study of Lenvatinib in Patients With RET Fusion-Positive Lung Adenocarcinoma[J]. Lung Cancer (2019) 138:124–30.
2.Drilon A, Rekhtman N, Arcila M, et al.Cabozantinib in Patients With Advanced RET-Rearranged Non-Small-Cell Lung Cancer: An Open-Label, Single-Centre, Phase 2, Single-Arm Trial[J]. Lancet Oncol (2016) 17:1653–60.
3.Yoh K, Seto T, Satouchi M, Nishio M, et al.Vandetanib in Patients With Previously Treated RET-Rearranged Advanced non-Small-Cell Lung Cancer (LURET): An Open-Label, Multicentre Phase 2 Trial[J]. Lancet Respir Med (2017) 5:42–50.
4.Horiike A, Takeuchi K, Uenami T, et al.Sorafenib Treatment for Patients With RET Fusion-Positive Non-Small Cell Lung Cancer l[J]. Lung Cancer (2016) 93:43–6.
5.Nicholas W Choong, Mark Kozloff, David Taber, et al.Phase II study of sunitinib malate in head and neck squamous cell carcinoma[J]. Invest New Drugs. 2010 Oct;28(5):677-83.
6.Scott M. Wilhelm,Jacques Dumas,et al.Regorafenib (BAY 73-4506): A new oral multikinase inhibitor of angiogenic, stromal and oncogenic receptor tyrosine kinases with potent preclinical antitumor activity[J]. Int J Cancer. 2011 Jul 1;129(1):245-55.
7.Yajuan Lv,Jiandong Zhang, Fengjun Liu,et al.Targeted therapy with anlotinib for patient with recurrent glioblastoma.A case report and literature review[J]. Medicine (Baltimore). 2019 May; 98(22): e15749.
8.B. Brandhuber, J. Haas, B. Tuch,et al.The development of LOXO-292, a potent, KDR/VEGFR2-sparing RET kinase inhibitor for treating patients with RET-dependent cancers[J]. European Journal of Cancer, 69, S144.
9.Gautschi O, Milia J, Filleron T, Wolf J, Carbone DP, Owen D, et al. Targeting RET in Patients With RET-Rearranged Lung Cancers: Results From the Global, Multicenter RET Registry[J]. J Clin Oncol (2017) 35:1403–10.
10.Lee SH, Lee JK, Ahn MJ, et al. Vandetanib in Pretreated Patients With Advanced Non-Small Cell Lung Cancer-Harboring RET Rearrangement: A Phase II Clinical Trial[J]. Ann Oncol (2017) 28:292–7.
11.Drilon A, Hu ZI, Lai GGY, et al. Targeting RET-driven cancers: lessons from evolving preclinical and clinical landscapes[J]. Nat Rev Clin Oncol 2018;15(3):151–167.
12.Chang Lu, Xiao-Rong Dong, Jun Zhao, et al. Association of genetic and immuno-characteristics with clinical outcomes in patients with RET-rearranged non-small cell lung cancer: a retrospective multicenter study[J]. J Hematol Oncol. 2020 Apr 15;13(1):37.
13.ClinicalTrials.gov beta website. ++NSCLC&term=&cntry=&state=&city=&dist=.
14.Leylah M. Drusbosky, Estelamari Rodriguez, Richa Dawar,et al.Therapeutic strategies in RET gene rearranged non-small cell lung cancer. J Hematol Oncol. 2021; 14: 50.
15.Gainor JF, Curigliano G, Kim D-W, et al.Registrational Dataset From the Phase I/II ARROW Trial of Pralsetinib(BLU-667) in Patients (Pts) With Advanced RET Fusion+ Non-Small Cell Lung Cancer (NSCLC). J Clin Oncol (2020) 38:9515–5.
16.Umair Majeed, Rami Manochakian, Yujie Zhao,et al. Targeted therapy in advanced non-small cell lung cancer: current advances and future trends[J]. J Hematol Oncol. 2021; 14: 108.
17.Fu-Bin Zhu, Qi-Heng Gou and Lin-Yong Zhao.The Efficacy and Safety of RET-selective Inhibitors for Cancer Patients[J]. Journal of Exploratory Research in Pharmacology 2021;6(1):16-22.
18.Roberto Ferrara, Nathalie Auger, Edouard Auclin, et al. Clinical and Translational Implications of RET Rearrangements in Non-Small Cell Lung Cancer[J]. J Thorac Oncol. 2018 Jan;13(1):27-45.
限 时 特 惠: 本站每日持续更新海量各大内部创业教程,一年会员只需98元,全站资源免费下载 点击查看详情
站 长 微 信: lzxmw777






